新闻资讯
咨询热线
020-95984501传真:020-45987410
《Nature microbiology》综述 用于传染病研究的器官芯片模型
仅供医学专业人士阅读参考
在微生物感染过程中,病原体、宿主组织、免疫系统和微生物群落之间的相互作用起着重要作用,使得这些过程变得复杂难以研究。全球医疗系统面临着与抗微生物药物抗性上升以及新兴病原体相关的机会性感染数量增加的挑战。因此,需要深入了解微生物感染,以促进新的诊断工具和治疗方法的发展。传统上,对微生物病原体的研究主要依赖于动物和细胞培养模型来模拟宿主中的感染过程。近年来,微流控和生物工程的进展导致了器官芯片(Organ-on-chip,OoC)技术的发展。这些微流控系统创造了更具生理学意义的条件,并可被视为体外的人体化模型。
来自德国莱布尼茨天然产物和感染生物学研究所-汉斯诺尔研究所的Bernhard Hube团队综述了各种OoC模型及其在传染病研究中的应用。概述了使它们成为微生物学中有价值的工具的特性,如动态微环境、血管化、接近生理组织结构和功能免疫细胞的部分整合,以及它们的局限性。最后,讨论了OoC的前景及其在未来传染病研究中的潜在作用。相关工作以题为“Organ-on-chip models for infectious disease research”的综述文章发表在2024年03月25日的国际顶级期刊《Nature microbiology》。


1. 主要内容
本综述回顾了OoC模型的特点及其在传染病研究中的价值。讨论了这些模型在微生物致病性、宿主-病原体相互作用和治疗方法等方面的应用。目的是向传染病学家介绍OoC模型,并强调它们如何像动物模型一样为微生物发病机制提供有用的见解,同时保持体外系统的控制性和灵活性。
【OoC模型的特点】

大多数OoC模型是大约与显微镜玻片大小相当的细胞培养腔室,由一个或多个由膜或水凝胶分隔的隔室组成(图1a)。它们由光学透明材料制成,以便进行显微镜观察,并与微流控系统集成,通过培养腔室中灌注培养基,或通过真空泵对腔室进行拉伸和收缩(图1b)。通过在OoC模型的隔室中种植不同类型的细胞,可以模拟与特定研究问题相关的不同组织(图1c)。例如,可以包括类似血管系统的隔室,以研究免疫细胞的招募或病原体的传播。尽管这些特点在动物模型和某些体外模型中也存在,但在单个体外模型中结合人类细胞和生物力学力和支架等微环境特征,使OoC装置成为人类传染病研究中具有吸引力的研究系统(图1d)。实际上,在适当的动物模型缺失时,OoC模型可能非常重要。例如,抗体TNT005旨在治疗慢性炎症性脱髓鞘性多神经病(一种神经自身免疫性疾病),在OoC模型的临床前测试后获得了进行人体临床试验的批准,因为该疾病的动物模型不可用。这可能适用于严格的人类病原体或缺乏可访问或合适的动物模型的病原体。因此,使用人类细胞的先进体外模型是一种非常有价值的研究工具。
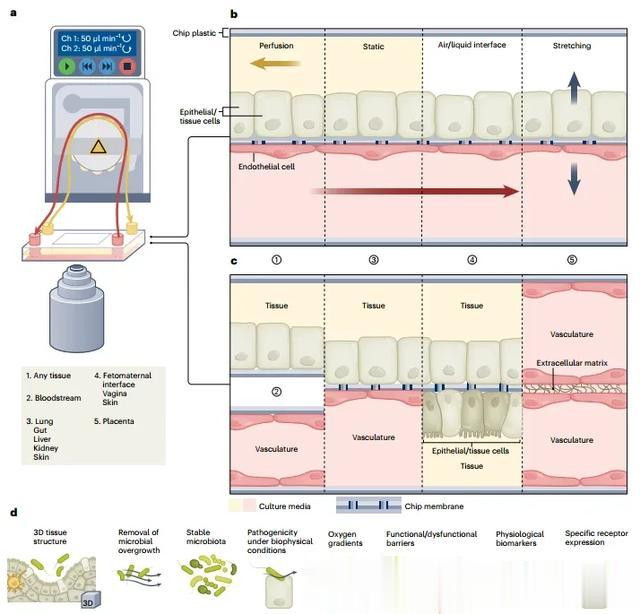
图1 一般的OoC模型
【OoC模型在传染病研究中的潜力】
在OoC模型中已经复制了几种与研究传染病相关的组织(图1c和图2)。皮肤和黏膜组织可以更准确地复制,因为它们通常具有较少的结构和功能复杂性。然而,随着生物复杂性的增加,更难在体外重新创建完整的器官功能。为解决这个问题,研究人员已经开始将重点放在小的功能单位上,而不是整个器官,例如神经血管单元与大脑。OoC装置已被用于模拟由病毒、细菌、真菌和寄生虫引起的感染(图2)。皮肤、肠道和肺等器官是主要关注的对象,因为它们通常是病原体入侵的第一接触点。肝脏、大脑和肾脏等经常受到感染的器官也可以部分地在OoC中建模。OoC模型在研究利用特定细胞受体(如许多病毒)和穿越组织屏障的致病因子方面特别有用。这导致了成熟的模型,已应用于基础感染研究和药物测试。OoC模型可以用于弥合传统细胞培养模型和动物模型之间的特定差距,例如,在体外模型的受控环境中结合体内发现的生理相关特征与人类细胞相结合。此外,OoC与显微镜的兼容性使得能够以比体内更高的时空分辨率观察过程,这已被利用来监测、表征和量化感染。然而,与任何模型一样,在使用之前必须了解其局限性。与OoC相比,动物模型在研究影响多个器官或适应性免疫反应(如败血症)的条件或结果时表现更好。与OoC相比,传统的细胞培养或器官样系统更容易应用于高通量方法。关键是要确定OoC可以发挥作用的研究目标,特别是因为所需的专业知识和技术挑战可能与动物实验相当。
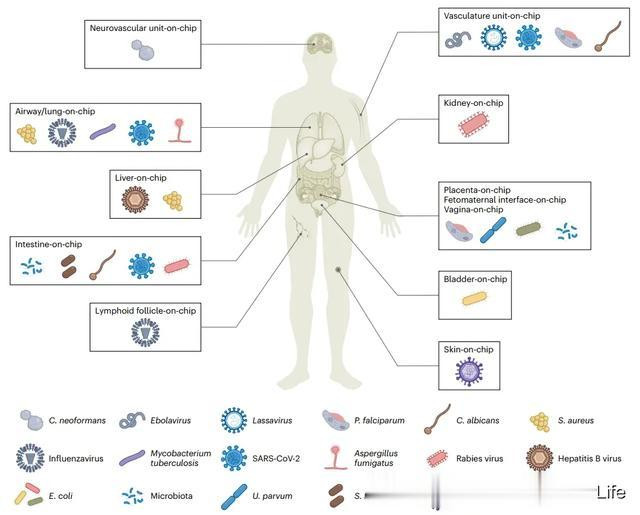
图2 感染生物学中的 OoC 模型
【在OoC模型中对生物物理宿主特性进行建模】
在OoC模型中的流动也允许评估组织间的相互作用。例如,在胎儿-母体界面模型中,连接了各种母体和胎儿细胞层,并进行了灌流。这使得可以研究细菌在母体子宫颈和胎儿组织上引起的上皮感染(图3a)。研究了免疫反应、Ureaplasma parvum感染细胞释放的外泌体的作用以及警报蛋白的作用,并确定了早产的生物标志物。许多微生物复制速度很快,使用静态模型具有挑战性。微生物可以快速过度生长宿主细胞,在培养基中消耗营养物质,最终杀死宿主细胞,而不诱导与体内观察到的表型相对应的现象。典型的解决方案包括防止细胞损伤的培养基、定期更换培养基、较短的实验时间或使用抗生素,但这可能会导致结果偏差。相比之下,OoC模型中的连续流动可以去除非粘附的微生物,防止微生物过度生长对模型的有害影响。这既可以研究快速增殖微生物的致病机制,又可以整合稳定的共生微生物群落。后者对于研究微生物群落尤其重要,因为它可以调节宿主免疫系统,并影响许多病原体的生长和毒力。与此一致,几种OoC模型已经证明了微生物群落对宿主的益处,例如预防感染和减轻炎症。
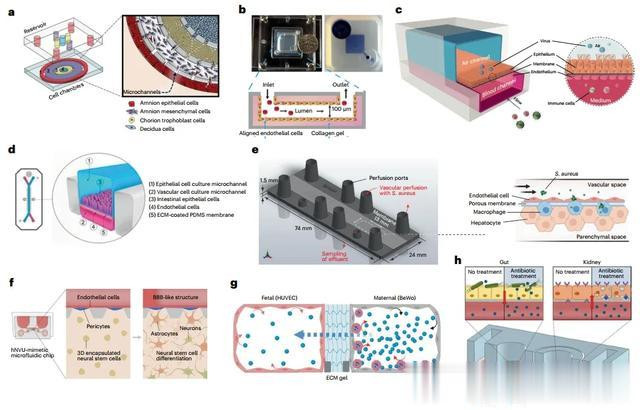
图3 传染病研究中使用的示例性 OoC 模型
【器官芯片模型中的血管化】
在OoC设备中应用流动的一个主要优势是将血管系统整合到组织模型中(图1b、c)。因此,可以研究病原体通过血液传播、免疫细胞的招募或药物的分布。在感染生物学领域使用的许多OoC模型通过用内皮细胞覆盖其中一个隔室来实现血管化。尽管还有其他方法可以实现血管化(例如,癌症研究通常需要更复杂的血管网络),但单一的专用通道更容易建立和操作,并且足以提供对感染过程独特的解释。
血管芯片模型(图3b)可用于研究血液传播的病原体与血管系统的相互作用,以及破坏血管完整性的病原体(如出血病毒)。通过注射荧光白蛋白并结合时间推移显微镜技术,已经研究了埃博拉病毒和拉沙病毒引起的血管病变。埃博拉病毒样颗粒导致血管渗漏并激活与疾病严重并发症相关的Rho-ROCK通路。进一步对Rho-ROCK通路的研究发现了在临床相关浓度下逆转血管渗漏的分子。
为研究特定的宿主-病原体相互作用,重现微血管的三维结构、生物标志物和物理特性具有重要意义。当恶性疟原虫感染的红细胞在脑部微血管中滞留时,会导致脑型疟疾。使用灌流的三维脑部微血管模型,确定了介导疟原虫感染红细胞与内皮细胞黏附的两种蛋白质。许多病原体可以通过血液传播到其他器官,引起威胁生命的全身性疾病。通过具有血管隔室的OoC可以模拟这个过程并研究分子机制(图3c-e)。例如,当白念珠菌从肠道进入血液循环时,可以引起全身性念珠菌病。在具有血管隔室的肠道芯片中,模拟了真菌生长、形态变化、组织损伤和迁移(全身性念珠菌病的特征)。使用这种方法量化了病原体侵入血管的程度,并进一步证明有益菌可以预防全身性念珠菌病。
【将功能性免疫细胞整合到OoC模型中】
将循环的先天免疫细胞(如中性粒细胞)可以通过OoC设备中的血管隔室进行灌流,以模拟趋化性、通过内皮屏障的迁移、组织浸润和与病原体的相互作用(图4a)。中性粒细胞的动态行为,包括中性粒细胞外网(neutrophil extracellular trap,NET)的形成和群聚,通过活体细胞成像显示,当免疫细胞浸润膀胱组织以清除尿路致病性大肠杆菌。中性粒细胞的招募和反应也在肺部和皮肤芯片模型中模拟了病毒感染。同样,单核细胞在经血管化的肝芯片中显示出在败血症后恢复肝功能的能力。通过血管隔室灌注单核细胞,它们附着在内皮细胞上,浸润了模型中的肝组织部分,并在急性炎症期间改善了肝细胞功能,从而重现了这些体内过程。OoCs还是研究黏膜免疫学和上皮组织与先天免疫细胞之间相互作用的有前景的平台。例如,组织驻留巨噬细胞对组织稳态至关重要,并通过释放细胞因子和感知其他细胞类型释放的细胞因子在炎症和病原体防御中发挥关键作用(图4a)。出于这个原因,巨噬细胞已经被整合到各种OoC模型中以研究宿主-病原体相互作用(图4a)。在将它们引入OoC模型之前,巨噬细胞可以相应地分化为感兴趣的亚群,例如巡游肺泡组织的肺泡巨噬细胞(图4a)。然而,细胞也可以在设备内分化,以模拟它们自然发展为各种细胞群体,如在肠道芯片模型中所示。在这里,单核细胞分化为组织驻留巨噬细胞和腔内采样树突状细胞。对内毒素的反应在血管和肠道隔室之间有所不同;在血管隔室中观察到内毒症(血液中存在细菌内毒素或脂多糖),而在肠道隔室中内毒素被“耐受化”(图4b)。因此,含有功能性先天免疫细胞的肠道OoC可以帮助模拟与炎症性疾病相关的肠道屏障生理和免疫病理学的重要方面。在OoC模型中也模拟了炎症性肠病(IBD)的临床特征,如由干扰素-γ等促炎细胞因子引起的绒毛损伤和肠道屏障破坏,以及对肠道隔室中细菌过度生长的反应(图4b)。
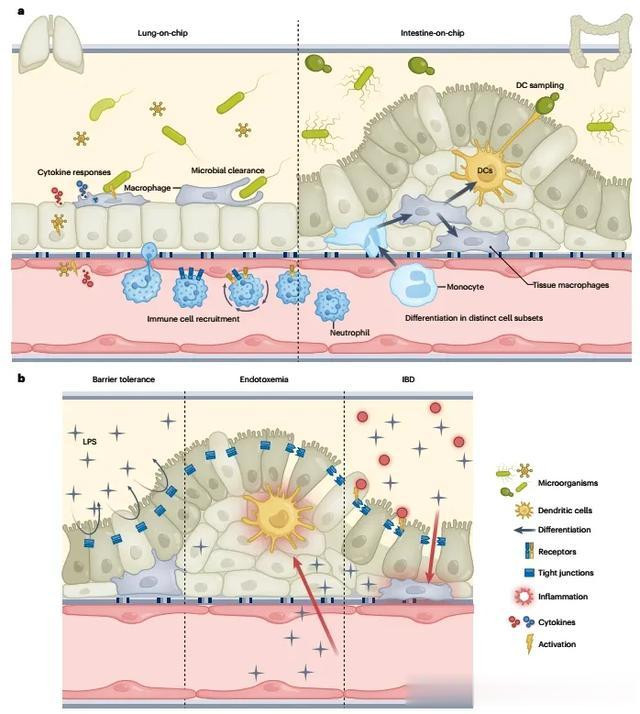
图4 将功能性免疫细胞整合到 OoC 模型中
【利用OoC模型对多器官感染进行建模】
微流体学隔室(Microfluidic compartments)可以连接在一起,将多个不同的组织整合到一个平台中,形成多器官芯片(MOoC)模型。这样的MOoC平台可以研究与全身性感染相关的研究问题,包括循环免疫细胞的作用或器官间的代谢产物交换。例如,肠-肾或肝-肾MOoC可能有助于研究全身性念珠菌感染,皮肤-肝平台可以模拟金黄色葡萄球菌感染。一个现有的例子是疟疾芯片模型。恶性疟原虫具有涉及多个人体器官的复杂生命周期。这个包含内皮细胞、脾脏、肝脏和循环红细胞的MOoC模型可以维持感染八天,并再现恶性疟原虫感染的各个阶段,同时展示对治疗的敏感性和耐药性。因此,它可以作为研究疟疾致病机制和测试抗疟药物的重要资源。
【OoC 系统的局限性】
· 在过去几年中,OoC模型在未来研究中的重要性不断增加,但它们仍然存在一些限制。一个主要挑战是需要标准化和验证,这是将这些模型纳入临床前研究的先决条件。目前,许多努力都致力于标准化OoC模型。
· 此外,许多芯片中使用的材料可能对药物发现流程构成挑战。聚二甲基硅氧烷(PDMS)是一种广泛使用的材料,用于制造芯片,因为它具有灵活性、透明度、多功能性和易于使用的特点。然而,PDMS会吸收疏水分子,并诱导蛋白质吸附到其表面。其他用于管道或储液池的塑料可能会产生相同的效果。这可能会改变培养基中分子的浓度分布,对结果产生负面影响。此外,分离和结构化细胞的人工膜或支架会限制趋化因子、代谢产物和微生物在组织之间的扩散和交换。
· 与其他模型(如孔板或器官样)相比,OoC模型通常吞吐量较低。这使得它们不太适合筛选候选药物,并限制了它们在管道的后续阶段中的应用,因为只有少数主导化合物留下。k1体育官网
· OoC模型可能并不适合每个研究机构。它们比传统的细胞培养模型更难处理,并且需要特定的设备和材料,这可能增加实验的成本。它们的复杂性较高(如不同的细胞类型、组织结构和机械力),在解剖分子或细胞水平的相互作用时可能会带来一些不利因素,因为需要考虑更多的变量。
· 最后,OoC模型无法完全取代动物模型,因为仍然需要这些模型来评估系统性结果和整体过程。大多数疾病和治疗不仅仅局限于单个细胞间的相互作用,而是涉及多个组织和器官。OoC可以重新构建几种组织和结构,但无法完全再现人体的高度复杂性。
2. 总结与展望
在这里提到的各种研究表明,OoC模型可以帮助再现人体组织的构成、结构、功能和环境。尽管其中一些优点并非是OoC模型独有的,但它们将许多优势融合到一个平台中,使其能够处理感染生物学中的复杂研究目标,同时保持体外工作的灵活性和可控性。需要注意的是,OoC模型本身并不比其他模型更优越,但它们为体外系统和体内模型提供了另一种选择。事实上,使用不同的模型来解决研究问题的特定部分是一种常见的方法。在正确的研究问题上,OoC模型可以成为强大的工具。它们特别适用于模拟动态环境或多个组织之间的相互连接的传染病。OoC模型可以灵活地设计和调整,以适应科学或工业需求。当前市场上也提供了具有不同复杂度、多功能性、易用性和价格的OoC模型。然而,是否使用OoC模型以及选择哪种类型应该根据具体情况考虑,并结合讨论的要点进行决策。
总的来说,(M)OoC在感染生物学、免疫学和生物医学领域正在蓬勃发展。在未来几年,我们可以预期不同(M)OoC格式和应用的发展,以模拟健康和疾病。考虑到它们日益多样、复杂和可靠的结果,它们将为传染病提供新的见解,并有望帮助发现新的抗感染化合物。k1体育app
了解更多
关注“EngineeringForLife”,了解更多前沿科研资讯

k1体育官网



